La Agencia Europea de Medicamentos (EMA) avaló que se aplique la tercera dosis de la vacuna contra el coronavirus Pfizer/BioNTech en personas mayores de 18 años, consecuencia de la preocupación porque disminuya la eficacia de la misma tras las primeras dos aplicaciones.
“Las dosis de refuerzo de Comirnaty pueden considerarse para personas de 18 años en adelante, al menos seis meses después de la segunda dosis”, puntualizó la Agencia Europea.
Aunque la aplicación de una tercera dosis, se puntualizó que serán tomada por los organismos de salud pública nacionales.
Por otra parte, aclaró que no se conoce el riesgo de enfermedades cardíacas inflamatorias u otros efectos secundarios tras la aplicación del refuerzo, aunque son muy raros los casos que se han presentado de inflamación del músculo cardíaco en personas que recibieron el biológico.
De acuerdo con la información de la farmacéutica, la efectividad del biológico es de 95%, mientras que de Moderna es de 94.5%; Sputnik V de 91.6%: Novavax de 89%; AstraZeneca de 70%, Janssen de 66% y Sinovac de 50 por ciento.
La EMA también dio el aval para que se suministra la tercer vacuna de Moderna o Pfizer en personas con sistemas inmunitarios frágiles y su aplicación sería 28 días posterior a la segunda dosis.
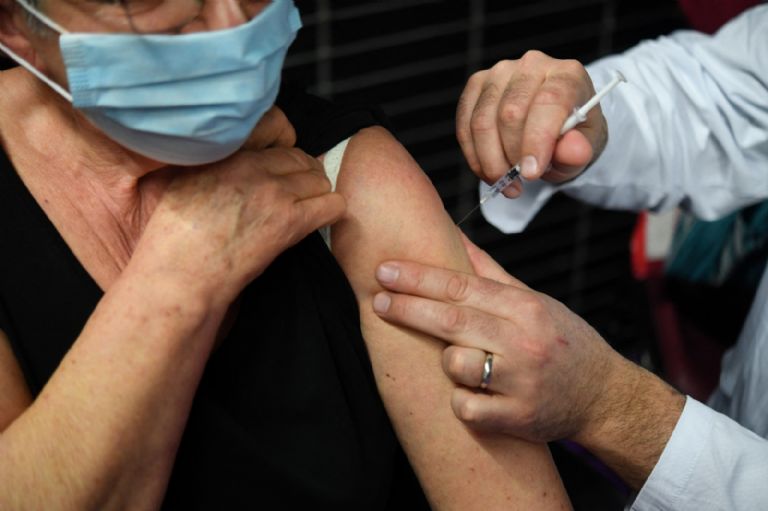
CDC recomienda aplicación de una tercera dosis a adultos mayores
Cabe señalar que Estados Unidos, el Comité Asesor de Inmunización de los Centros para el Control y la Prevención de Enfermedades (CDC, por su sigla en inglés) aprobó la aplicación de la tercera dosis el pasado 18 de septiembre pero solo en personas mayores de 65 años y población de alto riesgo.
La recomendación ocurrió un día después de que la Administración de Alimentos y Medicamentos (FDA, por su sigla en inglés) autorizó de emergencia la dosis de refuerzo de dicho biológico.
En un comunicado que emitió la FDA, indicó que se modifica la autorización de uso de emergencia para la vacuna COVID-19 de Pfizer-BioNTech”, con lo cual quedaba permitido la aplicación de una dosis de refuerzo, “debe administrarse al menos seis meses después de completar el primer esquema”.
Te puede interesar: ISSSTE está listo para vacunar a población de 12 a 17 años; tienen registro de 21 mil menores con comorbilidades















